17.600 Studienteilnehmer
England: Abnehm-Spritze Wegovy für Herzinfarkt-Prävention zugelassen
Die britische Regulierungsbehörde für Arzneimittel und Gesundheitsprodukte (MHRA) hat ein Medikament zur Gewichtsreduktion für einen neuen Zweck zugelassen. Und zwar zur Verringerung des Risikos von Herzproblemen bei Menschen mit Übergewicht und Fettleibigkeit.
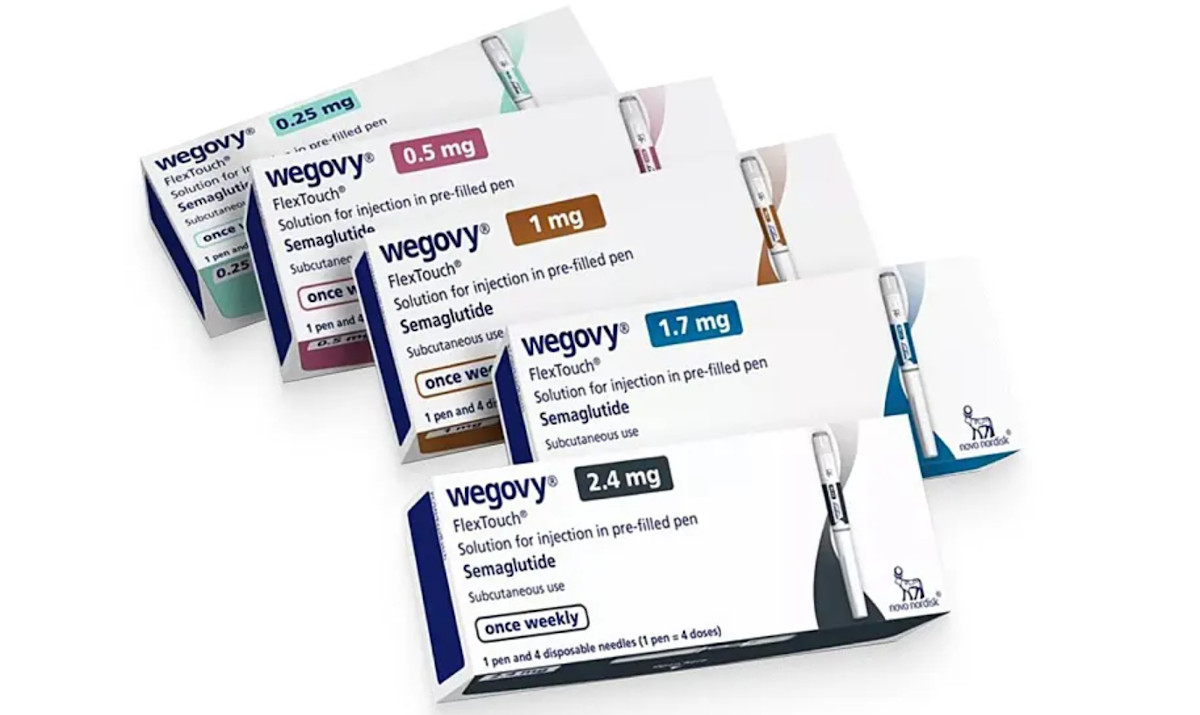
„Wegovy“ ist damit das erste Medikament zur Gewichtsreduzierung, das im Vereinigten Königreich als vorbeugende Behandlung für Menschen mit einer – so die MHRA – „etablierten Herz-Kreislauf-Erkrankung“ zugelassen ist.
Konkret bedeutet die Neuregelung, dass das Medikament Menschen mit einem Body-Mass-Index (BMI) von 27 oder mehr verschrieben werden kann, bei denen bereits entsprechende Probleme diagnostiziert worden sind.
Das auf dem Antidiabetikum Semaglutid basierende Medikament bewirkt bei Konsumenten ein Sättigungsgefühl. Daher wird es in Großbritannien zur Behandlung von Fettleibigkeit verschrieben, in Verbindung mit der Empfehlung zu Diätkost, körperlicher Betätigung und Verhaltensanpassung.
Ausschlaggebend für die MHRA-Entscheidung war laut Guardian eine neue Studie, die zu dem Ergebnis kommt, dass Wegovy das Risiko für schwere kardiovaskuläre Ereignisse wie Herzinfarkte und Schlaganfälle signifikant senken kann.
“Wichtiger Schritt zur Bekämpfung der schwerwiegenden Folgen von Fettleibigkeit“
Konkret wurde bei der Untersuchung 17.600 Studienteilnehmern Wegovy oder ein Placebo verschrieben. Die Forscher stellten fest, dass das von Novo Nordisk hergestellte Präparat das Risiko schwerer kardiovaskulärer Ereignisse um rund 20 Prozent senkte.
Die MHRA-Zulassung ist ein Schritt auf dem Weg zur Verwendung des Medikaments im staatlichen Gesundheitsdienst. Bevor es in großem Umfang im Gesundheitswesen eingesetzt wird, muss es noch vom National Institute for Health and Care Excellence (Nizza) bewertet werden.
Shirley Hopper, stellvertretende Direktorin für innovative Arzneimittel bei der MHRA, sagte dazu: „Wir sind sicher, dass die für die Zulassung dieses Arzneimittels erforderlichen Standards hinsichtlich Sicherheit, Qualität und Wirksamkeit erfüllt sind.“
„Diese Behandlungsmöglichkeit, die Herzkrankheiten und Schlaganfällen vorbeugt, ist ein wichtiger Schritt zur Bekämpfung der schwerwiegenden gesundheitlichen Folgen von Fettleibigkeit. Wie bei allen Arzneimitteln werden wir auch hier die Sicherheit genauestens überprüfen“, fuhr sie fort.